Conférence donnée par le Dr Jacques Guillet, Conseiller scientifique national de l’Association Française des Malades de la thyroïde
L’ancienne formule (Euthyrox) supprimée en 2020 ? Pas si simple !
Lévothyrox. Peut-on croire l’ANSM ?
- Affaire Médiator => défauts majeurs d’ indépendance de l’Afssaps vis-à-vis, notamment, des laboratoires pharmaceutiques
- Création de l’ANSM pour lui succéder.
- Négligences, imprudences, ambigüités, présentations et communication malhonnêtes, transparence insuffisante, démarche scientifique absente, comportement plus administratif que sanitaire, caractérisent l’ANSM autour de la nouvelle formule de Lévothyrox.
« Changement de formule et de couleur des boîtes et des blisters »
- 2 mars 2017: l’ANSM annonce la nouvelle formule. Meilleure stabilité +/-5% au lieu de 10%. Lactose remplacé par mannitol et acide citrique, à dose dépourvue d’effet notoire .
- « Aucun changement lié à la modification de formule n’est attendu pour les patients ». (Fiche médecins)
- Bioéquivalence « garantie d’une efficacité et d’une sécurité identiques à celle de l’ancienne formule. »
- Sauf que…5/7/2017 ANSM : réunion téléphonique obtenu par l’AFMT qui a lancé l’alerte, et VST
- 4 au 10 septembre sondage Quotidien du Médecin : 68% des médecins rapportent des effets indésirables
Crise et Autorités
- 6 septembre Le Figaro :1500 signalements. L’ANSM refuse de confirmer.
- 11 septembre : Ministre de la Santé en annonce 9 000 En cause, un défaut de communication… Alternatives.
- 14 septembre. ANSM directives aux Comités régionaux de pharmacovigilance (CRPV) pour coder les signalements, « afin de mieux respecter les règles européennes ». (Trop de signalements? )
- Malgré cela, 19 septembre : 15 000 signalements à partir des données de 16 des 31 CRPV…
- 31 411 au 17 avril 2018
La faute aux réseaux sociaux ?
- « Pétition contre le nouveau Levothyrox» (MesOpinions.com 24/06
Signatures : 58 000 (19/08), 157 000 (28/08), 180 000 (01/09), 260 000 (13/09)
- Pétition « rendez-nous l’ancienne formule » (SantéNatureInnovation.com)
100 000 signatures en qques heures; total 170 000
- => « numéro vert (gratuit) concernant le changement de formule de couleur des boîtes » saturé 50 ↗ 90 personnes répondent , discours formaté inadapté. ANSM 23/8.
- l’ANSM, sans prévenir, bascule systématiquement plusieurs milliers d’appels sur AFMT et ses bénévoles. Saturation des lignes. Y aurait-il volonté de nuisance ?
Banalisation et contradictions
- Comité Technique de Pharmaco Vigilance (CTPV) 10/10/2017 : Evènements Indésirables (EI) en nombre jamais vu, TSH dans les normes pour 2/3 => « autres facteurs qu’une dysthyroïdie »
- Mais 11 octobre 2017. Communiqué ANSM sur ces résultats du CTPV : EI rares « tous (…) témoignent d’un déséquilibre thyroïdien».
- Conclusions de la Mission flash 31/10/2017. Après un simulacre d’écoute des malades. « La crise du Levothyrox enfin résolue » : Bioéquivalence « parfaite à 0,3% près », défaut de communication, signaux faibles, nocebo et réseaux sociaux
Oublis ?
- Excipient : «Acheminer le principe actif vers son site d’action, contrôler son absorption par l’organisme » et pas seulement donner forme et couleur
- ANSM affirme :«garantie d’une efficacité et d’une sécurité identiques à celle de l’ancienne formule »
- Sauf que : ANSM Merck-Serono : «susceptible d’amplifier légèrement son action. Réévaluation TSH chez personnes à risque.
- HAS : « pas d’amélioration du service médical rendu (ASMR V) par rapport aux spécialités déjà inscrites »
Habillage médiatique d’affirmations sans preuve
- Bioéquivalence : parfaite par définition.
- « Mission pour améliorer l’information des patients et des professionnels de santé sur les médicaments » Magali Leo France Asso Santé, Dr Gérard Kierkzek urgentiste, Europe I France télévision, télé 7 jours. Sociologue. Pharmacien.Education thérapeutique
- «Effet nocebo» exclusif, lié aux réseaux sociaux
- Excipients : édulcorant du chewing-gum sans sucre et ingrédient des confitures industrielles.
- Alternatives : « rapidement progressive »
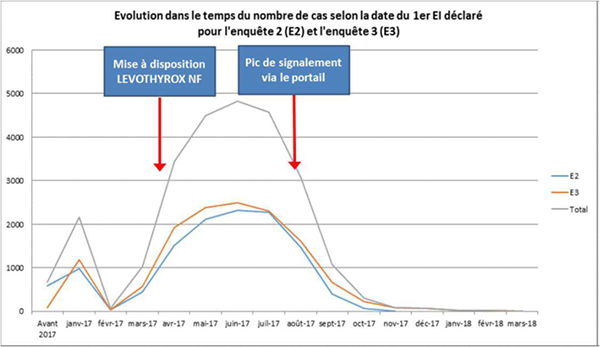
Réseaux sociaux ? Début des signalements bien avant
« Le 23 août 2017, (…) l’ANSM a mis en place un numéro vert (gratuit) concernant le changement de formule de couleur des boîtes de Lévothyrox. »
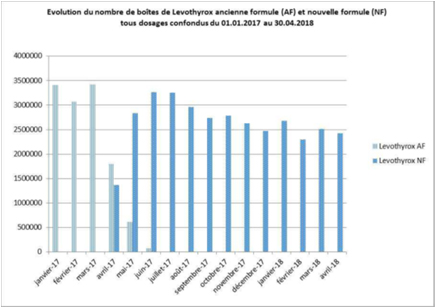
Mais 20 à 30% des malades fuient le Levothyrox NF
Levothyrox a subi une « Modification majeure de type II ».
Worksharing procedure, European Medicines Agency.
- « Changements qualitatifs ou quantitatifs concernant un ou plusieurs excipients, susceptibles d’avoir des répercussions significatives sur la sécurité, la qualité ou l’efficacité du médicament». CE/1234/200.
- « ces modifications doivent être approuvées par l’autorité compétente avant leur mises en œuvre. »
Démarche scientifique de l’AFMT ?
- Changement brutal imposé par l’ANSM à 3 millions de malades = conditions d’une étude quasi expérimentale
- Appels de l’AFMT aux Réunions ou Comités de suivi à partir de septembre et octobre 2017 :
- «La Recherche en thyroïdologie devrait s’engouffrer dans l’analyse des faits observés ». Liste des pistes énoncée.
- Inertie des autorités, oppositions des experts de la « croyance nocebo» à tout travail de Recherche. Minimisation.
- AFMT : Données pour la Recherche?
Etude de bioéquivalence
- Résumé présenté par l’ANSM au Comité de suivi où siège l’AFMT le 16 octobre 2017
- Autorisation de mise sur le marché n’est fondée que sur les résultats d’un Test de charge de 600 mg de Levothyrox AF et NF
- Mesure de la concentration de lévothyroxine totale (T4) pendant 72 heures dans le sérum de 204 volontaires sains. Majorité hommes jeunes
- Et comparaison des moyennes AF et NF
Bioéquivalence cliniquement irrecevable pour l’AFMT
- Dosage de T4 totale supplanté par T4 libre (environ 0,03% mais non proportionnelle) depuis les années 1980. T4 endogène et médicament non différenciée ni corrigée.
- TSH : paramètre de référence écarté
- Coefficients de variation (CV) des moyennes de T4 au pic et sous la courbe : supérieure à 17%
- Pourtant l’effectif important et les concentrations élevées réduisent mathématiquement les CV
- Pour une concentration cible de 100, les valeurs extrêmes de 66 et 134 sont considérées comme bioéquivalentes !
Recoupements avec l’échec des génériques 2010-2011
- Bioéquivalence pour lévothyroxine Biogaran et Robapharm/ Levothyrox AF
- Excipient dominant mannitol, comme dans Levothyrox NF, contrairement à l’AF (lactose)
- Nombreuses « difficultés » cliniques
- => ordonnances levothyrox « non substituable » après mise sous surveillance par l’AFSAPSS (ancêtre ANSM)
Etude scientifique 2019 => AF et NF non substituables
- Concordet et al réussissent à récupérer les données brutes de l’étude.
- Méthodologie scientifiquement irréprochable
- Clin Pharmacokinet 2019, 4 avril, complété en réponse à 2 lettres à l’éditeur
- 17% hors des limites acceptables sans ajustement (norme tolérée 10%).. Après ajustement, plus de 50%
- Pour cette équipe, le variabilité inter individuelle considérable fait que les deux formules ne sont pas substituables
Simple déséquilibre hormonal ?
- E.I. « amélioration … dans 65% des cas avec un changement de spécialité et dans 20% des cas avec une adaptation de dosage » Rapport Pharmacovigilance 25/1/2018
- Interactions méconnues ?
- Lots ó effets indésirables (étude AFMT) avec ou sans variation TSH ?
- Pourquoi 67% sans déséquilibre hormonal?…
- Limites du portail de pharmacovigilance ? symptômes parfois hâtivement intégrés, hyper-hypothyroïdie et combinés.
Excipients et réponse thérapeutique
- Dissolution des comprimés : NF (mannitol) plus lente qu’AF (lactose)
- Test de bioéquivalence, pharmacocinétique, différents selon l’acidité gastrique Seng Yu C, J Pharm Pharm Sci2015;18(5):844-55.
- Acidité↗dissolution cp mais inactive Levothyroxine sodique=>↘absorption de sa forme active
- ANSM n’a pas effectué de test de dissolution car les méthodes utilisées par Merck KGaA étaient différentes
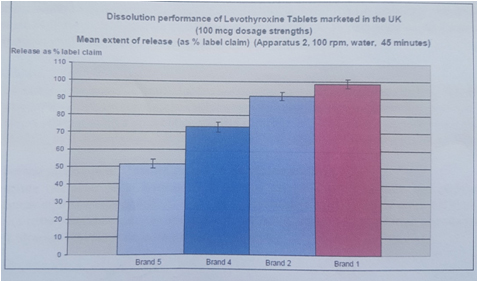
Regard britannique
- Etude normée sur les performances de dissolution des comprimés de levothyroxine sodique sur le marché britannique en 2013
- % libéré par rapport au % prétendu : comprimés de 100mg de marques différentes (MHRA 2013)
Levothyroxine, environnement
- MHRA, 7 janvier 2013 : « des modifications mineures de la formulation et de la fabrication peuvent avoir un impact majeur sur la sécurité et l’efficacité »
- Levothyroxine sodique pentathydratée stableàdiàmonohydrate àamorphe
- Levothyroxine sensible à : compression, lumière, O₂, humidité, température, certains matériaux comme le plastique et l’acier utilisés dans les machines (Patel 2003)
- Interférences d’impuretés non détectées avec les analyses normées de l’ANSM?
Regard belge. Takeda-Christiaens
- Procédés de fabrication des comprimés
- Influence de la compression
- Courrier en novembre 2014 pour 1er janvier 2015 AF compaction à NF granulation humide.
- Peu de différence AF NF Takeda
- Lactose identique 103 mg/cp
- AF hydrogénophosphate de calcium dihydrate à NF gélatine et talc
- Bioéquivalence 24 volontaires sains, correction des T4 endogènes individuelles,
- NF/AF : + 31 % en moyenne (AUC 0-72h – 90% intervalle de confiance [115,8-148,1])
- => étude clinique prospective, 84 malades, thyroïdectomie totale. TSH
- Chez 2/3 posologie modifiée (53↘ ,2↗)
- Courriers aux médecins , consultation initiale, TSH systématique, suivi médical
- Courrier aux pharmaciens :

Journal Officiel de l’Association Américaine des Scientifiques Pharmaceutiques
Nouvelles données sur les modifications à l’état solide du pentahydrate de sodium de lévothyroxine pendant la déshydratation et son lien avec l’instabilité chimique.
Stratégie de Recherche : profils d’impuretés NF/AF
- Constat : ANSM analyses normatives sur les NF d’officine
- Appel aux malades : faire parvenir à l’AFMT les comprimés AF et NF inutilisés.
- Couvrir l’AF et tous les lots NF incriminés
- Faire déterminer les profils d’impureté par des laboratoires d’analyse indépendants.
- Limiter les coûts (cotisation des malades), encourager et soutenir la Recherche scientifique.
Analyses AF/NF – Différence de profils
- Analyse de 11 des 50 principaux éléments de la classification périodique. Nickel absent de l’AF (Laboratoire français, mars 2018)
- Nanoparticules microscope électronique à balayage et micro analyse RX (Laboratoire italien, avril 2018).
- Chromatographie HPLC et colonne chirale (Laboratoire américain) : impureté dextrogyre seulement sur la NF, variant selon le lot, chromatographiquement proche et quasi incluse dans le pic de levothyroxine?
- ANSM systématiquement informée des résultats
Quel a été le coût du changement de formule pour la collectivité ?
- Souffrances des malades è 25 à 30% ont quitté le Lévothyrox NF.
- Coût financier pour la collectivité ?
Le rapport du SNDS démontre un surcoût considérable du switch Lévothyrox AF/NF
- Conséquences du passage à la nouvelle formule du Lévothyrox en France
- Etude de pharmaco-épidémiologie à partir des données du Système National des Données de Santé (SNDS)
- Rapport final juin 2019
Pas de différence de mortalité ?
- Rapport préliminaire 20/12/2018. Complet en juin 2019
- 1 037 553 malades AF versus NF par rapport à 248 304 Diabétiques II. -> perte de sensibilité de l’étude
- Etude sur 7,5 mois (ne correspond pas aux dates des actes médicaux)
- Indication du traitement inconnue pour 48,5%
- Malades <18 ans et > 65 ans écartés,
- Arrêts du traitement (décès..autre) remplacés par d’autres malades pour que le nombre reste constant
- En résumé, rapport biaisé établi sur des données tronquées.
Coût minimum en TSH et consultations (âge 18 à 65 ans) : 18 millions d’euros
- Durée 6 à 9 mois, moyenne 7,5 mois
- 20% quittent NF (alternatives à partir d’octobre)
- +31% TSH soit 1,17 AF/1,53 NF 8,10 euros X 0,36 X 3 millions
- <-> recommandations ansm ?
- Arrêts de travail>7j : +2%
- Consultations : +2%
- France 360 000 X 25 euros
- Benzodiazépines +4% en relatif
- Impacts accès aux soins sur la durée; 3 mois ?
- alternatives au compte-goutte. Chute de 20 à 30% des ventes.
- = 8,75 millions d’euros
- Recommandations ciblées sur <18 ans et >65 ans
- = diabétiques. <7j?
- ++ Août-Octobre 2017
- 9 millions d’euros + dépassements
- -2% (-6% chez diabète)
Switch Synthroid USA
- Journal of medical Economics 2018, 21:5,518-524 Abbvie
- Dans l’année qui suit le changement
- Coûts médicaux seuls et avec médicament
- En continuant le même médicament princeps
- 595 et 757 dollars
- en changeant
- 1023 et 1132 dollars
- +72% et + 50%
| Hypothyroïdie
Estimation |
Coûts directs | Coûts de perte de productivité | Coûts totaux |
| Aucune modification de dose a | $ 1091 | 492 $ | 1583 $ |
| Trois changements de dose ou plus a | $ 3194 | 916 $ | 4110 $ |
Adapté de Hallert 2014; Owens 2014; Dim 2014; Rachana 2014
In Frank R. Ernst et al Clin Drug Investig. 2017; 37(1): 71–83.
The Economic Impact of Levothyroxine Dose Adjustments: the CONTROL HE Study. Publié en ligne le 31 octobre 2016
Ordre de grandeur des surcoûts
- Près de 5% de la population française sous Levothyrox.
- > 65 ans (19,6% de la population) écartés
- Forte incidence des hypothyroïdies dans cette population : >14/1000 après 75 ans. Et fragilités fréquentes.
- En France, pas de changement du prix du médicament, plus de 18 millions d’euros de dépenses supplémentaires sur le seul poste consultations et dosages de TSH pour les 18-65 ans. Donc largement sous-estimé
- Coûts des actes médicaux différents entre France et USA => valeur relative seule utilisable, mais qui englobe les autres postes de dépenses
- Sur cette base : augmentation des dépenses de prise en charge de l’hypothyroidie de 72% dans l’année en conséquence d’un switch. Pourcentage probablement peu éloigné de la réalité française
- Et 293% en coût direct quand 3 switchs sont réalisés
Euthyrox « français » :122 000 patients
Euthyrox « étranger » : ?
- « Anticipation de la fin de la mise à disposition de la spécialité Euthyrox en 2020 (première moitié) » ANSM 18/11/2019
- Opposition de l’AFMT suivie par les autres associations pour éviter de nouveaux risques ou déséquilibres
- Introduction des signes cliniques, de la qualité de vie, de la valeur cible individuelle de la TSH, de la nécessité de consultation d’endocrinologie spécialisée en cas de difficulté sur la TSH
Conclusion
- Demande de moratoire , avec garantie de continuité aussi longtemps que l’Euthyrox restera fabriqué pour les autres pays du monde
- Responsabilité du ministre de la santé (médecin) engagée sur ce « switch » : « primum non nocere»
- Date initiale du changement obligatoire repoussée de 2019 à début 2020 puis novembre 2020
- Quel sera l’impact du coronavirus?